Szerző:
Frank Hunt
A Teremtés Dátuma:
13 Március 2021
Frissítés Dátuma:
1 Július 2024
Tartalom
Fontos mérni a víz pH-ját - savasságának vagy lúgosságának mértékét. A vizet azok a növények és állatok használják, amelyektől függünk, és mindennap iszunk. A víz pH-értéke jelezheti az esetleges szennyeződést, ezért a víz pH-jának mérése fontos közegészségügyi óvintézkedés lehet.
Lépni
1/3 módszer: pH-mérő használata
 Kalibrálja a szondát és a mérőt a gyári utasításoknak megfelelően. Lehet, hogy egy ismert pH-értékű anyaggal kell kalibrálnia a mérőt. A mérő az adott anyagnak megfelelően állítható be. Ha laboratóriumon kívül akarja tesztelni a vizet, ajánlott néhány órával a helyszíni tesztelés előtt elvégezni ezt a kalibrálást.
Kalibrálja a szondát és a mérőt a gyári utasításoknak megfelelően. Lehet, hogy egy ismert pH-értékű anyaggal kell kalibrálnia a mérőt. A mérő az adott anyagnak megfelelően állítható be. Ha laboratóriumon kívül akarja tesztelni a vizet, ajánlott néhány órával a helyszíni tesztelés előtt elvégezni ezt a kalibrálást. - Használat előtt öblítse le a szondát tiszta vízzel. Szárítsa meg tiszta ruhával.
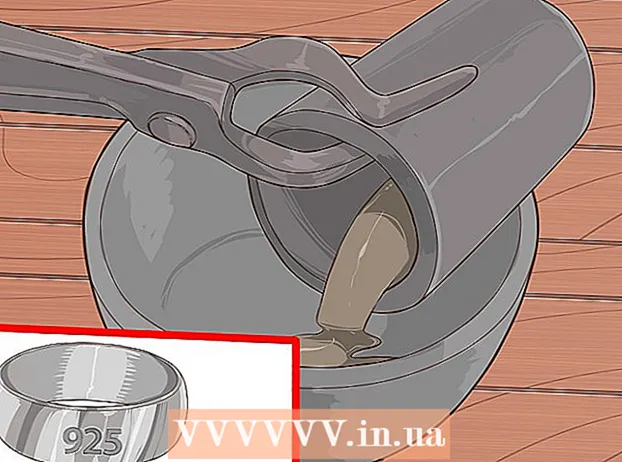
 Vegyen egy vízmintát, és öntse egy tiszta edénybe.
Vegyen egy vízmintát, és öntse egy tiszta edénybe.- A víznek elég mélynek kell lennie ahhoz, hogy az elektróda hegyét elmerítse.
- Hagyja a mintát egy ideig, hogy a hőmérséklet stabilizálódjon.
- Mérjük meg a minta hőmérsékletét hőmérővel.
 Állítsa be a mérőt a minta hőmérsékletével. A szonda érzékenységét a víz hőmérséklete befolyásolja, így a mérés csak akkor lehet pontos, ha megadja a hőmérsékleti adatokat.
Állítsa be a mérőt a minta hőmérsékletével. A szonda érzékenységét a víz hőmérséklete befolyásolja, így a mérés csak akkor lehet pontos, ha megadja a hőmérsékleti adatokat.  Helyezze a szondát a mintába. Várja meg, amíg a mérő eléri az egyensúlyt. A mérő stabil állapotban van, ha az olvasás stabil.
Helyezze a szondát a mintába. Várja meg, amíg a mérő eléri az egyensúlyt. A mérő stabil állapotban van, ha az olvasás stabil.  Olvassa el a minta pH-értékét. A pH-mérő 0–14 skálán adja az eredményt. Ha a víz tiszta, az értéke 7 körül van. Írja le megállapításait.
Olvassa el a minta pH-értékét. A pH-mérő 0–14 skálán adja az eredményt. Ha a víz tiszta, az értéke 7 körül van. Írja le megállapításait.
2/3 módszer: Lakmuszpapírral
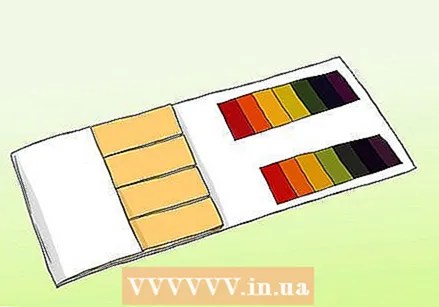 Ismerje meg a pH-papír és a lakmuszpapír közötti különbséget. PH-értékű papírt használhat a minta pontos leolvasásához. A pH-értékű papírt azonban nem szabad összetéveszteni a szokásos lakmuszpapírral. Mindkettő használható savak és bázisok tesztelésére, de fontos szempontokban különböznek egymástól.
Ismerje meg a pH-papír és a lakmuszpapír közötti különbséget. PH-értékű papírt használhat a minta pontos leolvasásához. A pH-értékű papírt azonban nem szabad összetéveszteni a szokásos lakmuszpapírral. Mindkettő használható savak és bázisok tesztelésére, de fontos szempontokban különböznek egymástól. - A pH-sávok egy sor indikátort tartalmaznak, amelyek oldatnak kitéve megváltoztatják a színüket. Az egyes rudak savainak és bázisainak erőssége eltér. A változás után a színminta összehasonlítható a készlethez mellékelt mintákkal.
- A lakmuszpapír savat vagy bázist (lúgot) tartalmazó papírcsík. A leggyakoribb csíkok a vörös (savval, amely reagál a bázisokkal) és a kék (a bázissal, amely savakkal reagál). A piros csíkok kék színűvé válnak, ha az anyag lúgos, és a kék csíkok pirosak, ha az anyag savas. A lakmuszpapírok gyors és egyszerű tesztként használhatók, de a legolcsóbb fajták nem mindig adják meg pontosan a megoldás erejét.
 Vegyünk egy mintát a vízből, és öntsük egy tiszta edénybe. A víznek elég mélynek kell lennie ahhoz, hogy a csíkot elmerítse.
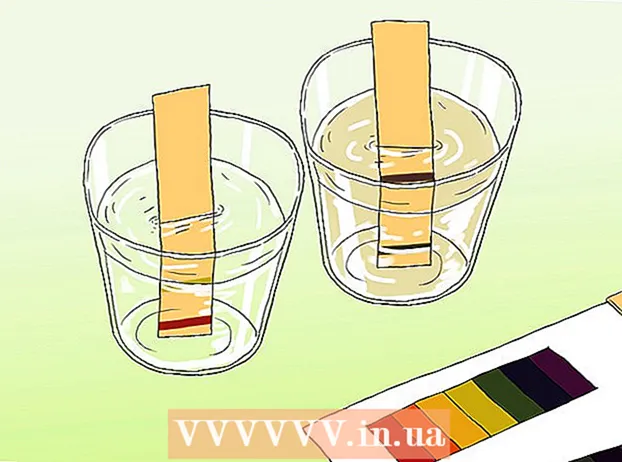
Vegyünk egy mintát a vízből, és öntsük egy tiszta edénybe. A víznek elég mélynek kell lennie ahhoz, hogy a csíkot elmerítse.  Tegyen egy tesztcsíkot a mintába. Néhány másodperces expozíció elegendő. A papír jelzősávjai néhány pillanat múlva megváltoztatják a színüket.
Tegyen egy tesztcsíkot a mintába. Néhány másodperces expozíció elegendő. A papír jelzősávjai néhány pillanat múlva megváltoztatják a színüket.  Hasonlítsa össze a tesztcsík végét a papírhoz kapott színskálával. A kártya színének vagy színeinek meg kell egyezniük a tesztcsík színével vagy színeivel. A színtérkép ezután a színmintákat a pH-szinthez kapcsolja.
Hasonlítsa össze a tesztcsík végét a papírhoz kapott színskálával. A kártya színének vagy színeinek meg kell egyezniük a tesztcsík színével vagy színeivel. A színtérkép ezután a színmintákat a pH-szinthez kapcsolja.
3/3 módszer: A pH megértése
 Ismerje meg, hogyan definiálják a savakat és bázisokat. A savasságot és lúgosságot (a bázisok leírásánál használt kifejezés) mind az általuk adományozott, mind a felvett hidrogénionok határozzák meg. A sav olyan anyag, amely hidrogénionokat adományoz (vagy "adományoz"), a bázis pedig olyan anyag, amely extra hidrogénionokat vesz fel.
Ismerje meg, hogyan definiálják a savakat és bázisokat. A savasságot és lúgosságot (a bázisok leírásánál használt kifejezés) mind az általuk adományozott, mind a felvett hidrogénionok határozzák meg. A sav olyan anyag, amely hidrogénionokat adományoz (vagy "adományoz"), a bázis pedig olyan anyag, amely extra hidrogénionokat vesz fel.  Értse meg a pH-skálát. A pH-értéket a vízoldható anyagok savasságának vagy lúgosságának mértékére használják. A vízben általában azonos mennyiségű hidroxidion (OH−) és hidroniumion (H3O +) található. A hidroxid- és hidroniumionok aránya akkor változik, ha savas vagy lúgos anyagot adunk a vízhez.
Értse meg a pH-skálát. A pH-értéket a vízoldható anyagok savasságának vagy lúgosságának mértékére használják. A vízben általában azonos mennyiségű hidroxidion (OH−) és hidroniumion (H3O +) található. A hidroxid- és hidroniumionok aránya akkor változik, ha savas vagy lúgos anyagot adunk a vízhez. - Általában 0 és 14 közötti skálának tekintik (bár az anyagok jócskán kívül eshetnek ezen a tartományon). A semleges anyagok pontszáma kb. 7, a savas anyagok 7 alatt vannak, az alkáli anyagok pedig 7 felett vannak.
- A pH-skála logaritmikus, vagyis az egész számbeli különbségek a savasságban vagy a lúgosságban tízszeres különbséget jelentenek. Például egy 2-es pH-értékű anyag tízszer savasabb, mint egy 3-as pH-értékű, és 100-szor savasabb, mint egy 4-es pH-értékű anyag. A skála ugyanúgy működik lúgos anyagokkal, bármilyen az egész szám tízszeres különbséget jelent.
 Tudja meg, miért teszteljük a víz pH-ját. A tiszta víz pH-ja 7, de a holland csapvíz pH-ja általában 7,5 és 8,3 között van. A nagyon savas víz (alacsony pH-értékű víz) nagyobb valószínűséggel oldja fel a mérgező vegyszereket. Ezek szennyezhetik a vizet, és veszélytelenné tehetik az ivást.
Tudja meg, miért teszteljük a víz pH-ját. A tiszta víz pH-ja 7, de a holland csapvíz pH-ja általában 7,5 és 8,3 között van. A nagyon savas víz (alacsony pH-értékű víz) nagyobb valószínűséggel oldja fel a mérgező vegyszereket. Ezek szennyezhetik a vizet, és veszélytelenné tehetik az ivást. - Általában ajánlott a pH-t a helyszínen tesztelni. Ha laboratóriumi kutatás céljából vízmintát vesz, a levegőből származó szén-dioxid (CO2) feloldódhat a vízben. Az oldott szén-dioxid reagál a víz ionjaival, és bázikus vagy semleges oldatokban növeli a savasságot. A szén-dioxid-szennyezés elkerülése érdekében a vizet a gyűjtéstől számított két órán belül meg kell vizsgálni.