Szerző:
Monica Porter
A Teremtés Dátuma:
22 Március 2021
Frissítés Dátuma:
1 Július 2024
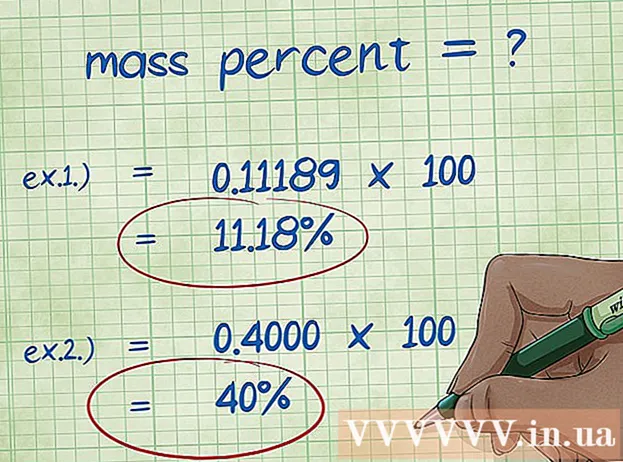
Tartalom
A tömegszázalék a kémiai vegyület egyes elemeinek százalékos arányát jelzi. A tömegszázalék megállapításához ismerni kell a vegyületben lévő elemek moláris tömegét grammban / mol vagy az oldatot alkotó anyagok grammszámát. A tömegszázalékot egy egyszerű képlet segítségével számítják ki, amely elosztja az elem (vagy oldott anyag) tömegét a vegyület (vagy oldat) tömegével.
Lépések
1/2 módszer: Számítsa ki a tömeg százalékát a tömeg ismeretében
Határozza meg a keverék tömegének százalékos egyenletét. A keverék tömegszázalékának kiszámításának alapképlete a következő: tömegszázalék = (minőségi tömeg / vegyes tömeg) x 100. Végül meg kell szorozni 100-zal a százalékos arány megjelenítéséhez.
- Írjon egyenletet, amikor elkezdi megoldani a problémát: tömegszázalék = (anyagtömeg / kevert tömeg) x 100.
- A probléma mennyisége megadja a minőség minőségét. Ha a témakör nem nyújt tájékoztatást, olvassa el a következő részt arról, hogy miként lehet megtalálni a tömegszázalékot súlyok ismerete nélkül.
- A keverék tömege megegyezik a keveréket vagy az oldatot alkotó anyagok teljes tömegével.

Számítsa ki a keverék tömegét. Miután megismerte az elemek vagy vegyületek tömegét, csak annyit kell tennie, hogy összeadja őket, hogy megkapja a végső keverék vagy oldat tömegét. Ez a nevező a tömegszázalék képletében.- 1. példa: Mennyi az 5 g nátrium-hidroxid tömegszázaléka 100 g vízzel feloldva?
- A keverék tömege a nátrium-hidroxid és a víz teljes tömege: 100 g + 5 g. Tehát a vegyes tömeg 105 g.
- 2. példa: Mekkora nátrium-klorid és víz szükséges 175 g 15% -os oldat elkészítéséhez?
- Ebben a példában, ahol ismeri a vegyes tömeget és a tömegszázalékot, a feladat arra kéri, hogy keresse meg a hozzáadott oldott anyag tömegét. A keverék tömege 175 g.
- 1. példa: Mennyi az 5 g nátrium-hidroxid tömegszázaléka 100 g vízzel feloldva?

Határozza meg az anyag tömegét a százalékos tömeg megállapításához. Amikor a kvíz megkérdezi az anyag "tömegszázalékának" megkeresését, meg kell találnia az anyag tömegét az összes összetevő teljes tömegének százalékában. Írja le az anyag tömegét, hogy megtalálja a tömeg százalékát. Ez a számláló a tömegszázalék képletében.- 1. példa: A nátrium-hidroxid tömege (tömegfrakcióval meghatározandó anyag) 5 g.
- 2. példa: Ebben a példában az anyag mennyisége az ismeretlen tömeg százalékos arányát keresi, és Ön keresi.

Cserélje ki a változókat a tömegszázalékos egyenletre. Miután meghatározta az egyes változók értékét, egyszerűen csatlakoztassa őket az egyenlethez.- 1. példa: tömegszázalék = (anyagtömeg / vegyes tömeg) x 100 = (5 g / 105 g) x 100.
- 2. példa: Át kell alakítanunk a tömegszázalékos egyenletet az ismeretlen minőségű mennyiség kiszámításához: minőségi tömeg = (tömegszázalék * vegyes tömeg) / 100 = (15 * 175) / 100 .
Számítsa ki a térfogat százalékát. Most, hogy az egyenlet kitöltődött, csak a tömegszázalékot kell kiszámítania. Osszuk el az anyag tömegét a keverék tömegével, majd szorozzuk meg 100-mal. Ez az anyag tömegszázaléka a keverékben.
- 1. példa: (5/105) x 100 = 0,04761 x 100 = 4,761%. Ezért 100 g vízben oldott 5 g nátrium-hidroxid tömegszázaléka 4761%.
- 2. példa: Az egyenlet a minőség mennyiségének kiszámításához történő átalakítás után (tömegszázalék * vegyes tömeg) / 100: (15 * 175) / 100 = (2625) / 100 = 26,25 gramm nátrium-klorid.
- A hozzáadott víz tömege a keverék tömege, levonva az anyag tömegét: 175 - 26,25 = 148,75 gramm víz.
2. módszer a 2-ből: Számítsa ki a tömegszázalékot, ha a tömeg nem ismert
Határozza meg a vegyület tömegszázalékának egyenletét! A vegyület tömegszázalékának kiszámításának alapképlete a következő: tömegszázalék = (elemi moláris tömeg / vegyület moláris tömege) x 100. Elemi moláris tömeg az egy mól elem tömege. míg a molekulatömeg egy mól vegyület tömege. Végül meg kell szorozni 100-mal, hogy megkapja a százalékos értéket.
- Írjon egyenletet, amikor elkezdi megoldani a problémát: tömegszázalék = (elemi moláris tömeg / vegyület moláris tömege) x 100.
- A fenti két érték mértékegysége gramm / mol (g / mol).
- Ha a probléma nem ad tömeget, akkor a moláris tömeg segítségével kiszámíthatja az elem tömegszázalékát.
- 1. példa: Számítsa ki a hidrogén tömegszázalékát egy vízmolekulában.
- 2. példa: Számítsa ki a szén tömegszázalékát egy glükózmolekulában.
Ír Kémiai formula. Ha a probléma nem terjed ki az egyes vegyületek kémiai képleteire, akkor le kell írnia őket. Ha a probléma a kémiai képlettel kapcsolatos, hagyja ki ezt a lépést, és folytassa az "Minden elem tömegének megkeresése" lépéssel.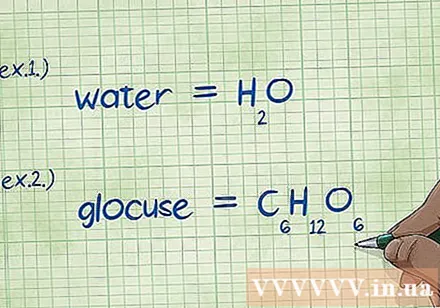
- 1. példa: Írja fel a víz kémiai képletét, H!2O.
- 2. példa: Írja fel a glükóz kémiai képletét, C6H12O6.
Keresse meg az egyes elemek tömegét a vegyületben. Keresse meg a kémiai képlet egyes elemeinek molekulatömegét a periódusos rendszerben. Az elemi tömeget általában a kémiai szimbólum alá írják. Írja le a vegyület egyes elemeinek tömegét!
- 1. példa: Megállapíthatjuk, hogy az oxigén tömegatomja 15,9994; és a hidrogén köbös atomja 1,0079.
- 2. példa: Megállapítottuk, hogy a szén tömegatomja 12 0107; oxigén értéke 15,9994; és a hidrogén 1,0079.
Szorozzuk meg a köbös atomot a mólaránnyal. Határozza meg a kémiai vegyület egyes elemeinek mólszámát (mólaránya). A mólarányt a vegyület kémiai képletében az alábbi kis számmal számoljuk. Szorozza meg az egyes elemek köbös atomját a mólaránnyal.
- 1. példa: A hidrogénnek két indexe van, míg az oxigénnek az indexe 1. Tehát megszorozzuk a hidrogén molekulatömegét 2-vel, 1,00794 X2 = 2,01588; és az oxigén molekulatömege 15,9994 (megszorozva eggyel).
- 2. példa: A szén indexe 6, a hidrogén 12, az oxigén pedig 6. Szorozzuk meg az egyes elemek köbös atomját az alábbi indexszel.
- Szén (12,0107 * 6) = 72,0642
- Hidrogén (1,00794 * 12) = 12,09528
- Oxigén (15,9994 * 6) = 95,9964
Számítsa ki a vegyület teljes tömegét. Adja hozzá a vegyület összes elemének tömegét. Kiszámíthatja a vegyületek teljes tömegét a moláris arányokban kifejezett tömegek felhasználásával. Ez a szám lesz a nevező a tömeg tömegegyenletében.
- 1. példa: 2,01588 g / mol (két mól hidrogénatom tömege) hozzáadása 15,9994 g / mol (egy mól oxigénatom tömege) hozzáadásához 18,01528 g / mol.
- 2. példa: Adja össze az összes súlyt: szén + hidrogén + oxigén = 72,0642 + 12,09528 + 95,9964 = 180,156 g / mol.
Határozza meg azt az elemi tömeget, amelyhez a tömegszázalékot ki kell számítani. Amikor a probléma "tömegszázalékot" kér, ez azt jelenti, hogy meg kell találnia egy adott elem tömegét a vegyületben az összes elem teljes tömegének százalékában. Határozza meg és írja le az elem tömegét. Ez a tömeg a mólarányban kifejezett tömeg. Ez a szám a százalékos tömegegyenlet számlálója.
- 1. példa: A hidrogén tömege egy vegyületben 2 01588 g / mol (két mol hidrogénatom tömege).
- 2. példa: A vegyületben a szén tömege 72,0642 g / mol (hat mól szénatom tömege).
Cserélje ki a változókat a tömegszázalékos egyenletre. Az egyes változók értékeinek meghatározása után egyszerűen cserélje ki őket az első lépésben azonosított egyenlettel: tömegszázalék = (elemi moláris tömeg / vegyület moláris tömege) x 100 .
- 1. példa: tömegszázalék = (elemi moláris tömeg / vegyület moláris tömege) x 100 = (2,1588 / 18,1528) x 100.
- 2. példa: tömegszázalék = (elemi moláris tömeg / vegyület moláris tömege) x 100 = (72,0642 / 180,156) x 100.
Számítsa ki a térfogat százalékát. Most, hogy az egyenlet kitöltődött, csak a tömegszázalékot kell kiszámítania. Osszuk el az elem tömegét a vegyület teljes tömegével, majd szorozzuk meg 100-val. Ez az elem tömegének százalékos aránya a vegyületben.
- 1. példa: tömegszázalék = (2,01588 / 18,01528) x 100 = 0,1111189 x 100 = 11,18%. Ezért a hidrogénatom tömegszázaléka a vízmolekulában 11,18%.
- 2. példa: tömegszázalék = (elemi moláris tömeg / vegyület moláris tömege) x 100 = (72,0642 / 180,156) x 100 = 0,4000 x 100 = 40,00%. Tehát a szénatom tömegszázaléka a glükózmolekulában 40,00%.