Szerző:
Eric Farmer
A Teremtés Dátuma:
10 Március 2021
Frissítés Dátuma:
1 Július 2024
Tartalom
- Lépések
- 1 /2 -es módszer: A neutronok számának meghatározása az atomokban (nem izotópok)
- 2. módszer 2 -ből: A neutronok számának meghatározása az izotópokban
- Tippek
Ugyanazon elem atomjaiban a protonok száma állandó, míg a neutronok száma változhat.Ha tudja, hogy egy adott atom hány neutront tartalmaz, akkor megállapíthatja, hogy szabályos atom vagy izotóp, amely kevesebb vagy több neutronnal rendelkezik. Az atomban lévő neutronok számának meghatározása meglehetősen egyszerű. Az atomban vagy izotópban lévő neutronok számának kiszámításához mindössze annyit kell tennie, hogy kövesse az utasításokat, és tartsa kéznél a periódusos rendszert.
Lépések
1 /2 -es módszer: A neutronok számának meghatározása az atomokban (nem izotópok)
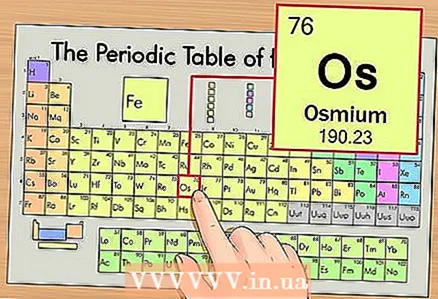 1 Keresse meg az elemet a periódusos rendszerben. Példaként figyelembe vesszük az ozmiumot (Os), amely a hatodik periódusban van (hatodik sor felülről).
1 Keresse meg az elemet a periódusos rendszerben. Példaként figyelembe vesszük az ozmiumot (Os), amely a hatodik periódusban van (hatodik sor felülről).  2 Keresse meg az elem atomszámát. Ez általában az elem cellájában a legszembetűnőbb szám, és általában a szimbóluma felett található (a példánkban használt periódusos rendszerben nincs más szám). Az atomszám a protonok száma az adott elem egyik atomjában. Az ozmium esetében ez a szám 76, vagyis egy ozmiumatomban 76 proton található.
2 Keresse meg az elem atomszámát. Ez általában az elem cellájában a legszembetűnőbb szám, és általában a szimbóluma felett található (a példánkban használt periódusos rendszerben nincs más szám). Az atomszám a protonok száma az adott elem egyik atomjában. Az ozmium esetében ez a szám 76, vagyis egy ozmiumatomban 76 proton található. - A protonok száma változatlan, és ez teszi az elemet elemmé.
 3 Keresse meg az elem atomtömegét. Ez a szám általában az elem szimbólum alatt található. Kérjük, vegye figyelembe, hogy a példánkban szereplő periódusos rendszer verziójában az atomtömeg nincs megadva (ez nem mindig van így; a periódusos rendszer sok változatában az atomtömeg van feltüntetve). Az ozmium atomtömege 190,23.
3 Keresse meg az elem atomtömegét. Ez a szám általában az elem szimbólum alatt található. Kérjük, vegye figyelembe, hogy a példánkban szereplő periódusos rendszer verziójában az atomtömeg nincs megadva (ez nem mindig van így; a periódusos rendszer sok változatában az atomtömeg van feltüntetve). Az ozmium atomtömege 190,23.  4 Kerekítse az atomtömeget a legközelebbi egész számra. Példánkban a 190,23 -at 190 -re kerekítik.
4 Kerekítse az atomtömeget a legközelebbi egész számra. Példánkban a 190,23 -at 190 -re kerekítik. - Az atomtömeg egy adott elem izotópjainak átlagos száma, általában nem egész számban fejezik ki.
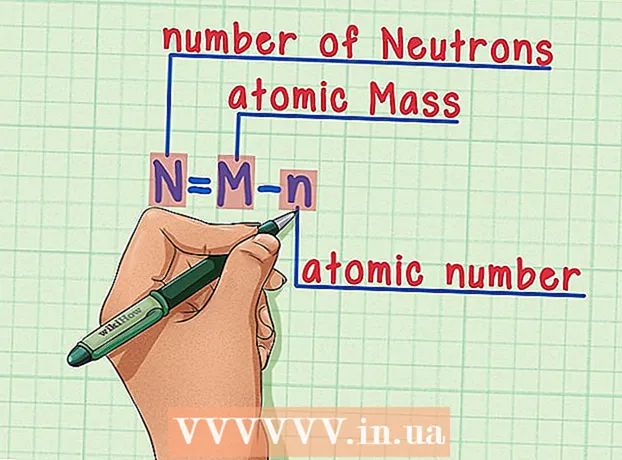
 5 Vonjuk le az atomszámot az atomtömegből. Mivel a protonok és a neutronok az atomtömeg abszolút részét teszik ki, az atomtömegből kivonva a protonok számát (vagyis az atomszámot, amely megegyezik a protonok számával), megadjuk az atomban lévő neutronok számát. A tizedesvessző utáni számok az atomban lévő elektronok nagyon kis tömegére vonatkoznak. Példánkban: 190 (atomtömeg) - 76 (protonok száma) = 114 (neutronok száma).
5 Vonjuk le az atomszámot az atomtömegből. Mivel a protonok és a neutronok az atomtömeg abszolút részét teszik ki, az atomtömegből kivonva a protonok számát (vagyis az atomszámot, amely megegyezik a protonok számával), megadjuk az atomban lévő neutronok számát. A tizedesvessző utáni számok az atomban lévő elektronok nagyon kis tömegére vonatkoznak. Példánkban: 190 (atomtömeg) - 76 (protonok száma) = 114 (neutronok száma). 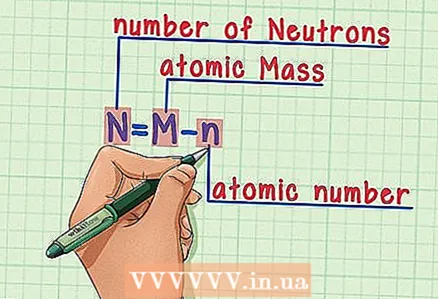 6 Ne feledje a képletet. A neutronok számának meghatározásához használja ezt a képletet:
6 Ne feledje a képletet. A neutronok számának meghatározásához használja ezt a képletet: - N = M - n
- N = neutronok száma
- M = atomtömeg
- n = atomszám
- N = M - n
2. módszer 2 -ből: A neutronok számának meghatározása az izotópokban
 1 Keresse meg az elemet a periódusos rendszerben. Példaként a 14C szén izotópját vesszük figyelembe. Mivel a 14C nem izotóp szén csak szén C, keresse meg a szenet a periódusos rendszerben (második periódus vagy második sor felülről).
1 Keresse meg az elemet a periódusos rendszerben. Példaként a 14C szén izotópját vesszük figyelembe. Mivel a 14C nem izotóp szén csak szén C, keresse meg a szenet a periódusos rendszerben (második periódus vagy második sor felülről).  2 Keresse meg az elem atomszámát. Ez általában az elem cellájában a legszembetűnőbb szám, és általában a szimbóluma felett található (a példánkban használt periódusos rendszerben nincs más szám). Az atomszám a protonok száma az adott elem egyik atomjában. A szén a 6 -os szám, ami azt jelenti, hogy egy szénnek hat protonja van.
2 Keresse meg az elem atomszámát. Ez általában az elem cellájában a legszembetűnőbb szám, és általában a szimbóluma felett található (a példánkban használt periódusos rendszerben nincs más szám). Az atomszám a protonok száma az adott elem egyik atomjában. A szén a 6 -os szám, ami azt jelenti, hogy egy szénnek hat protonja van.  3 Keresse meg az atomtömeget. Izotópok esetében ezt nagyon könnyű megtenni, mivel az atomtömegük szerint nevezik őket. Esetünkben a 14C szén atomtömege 14. Most már tudjuk az izotóp atomtömegét; a későbbi számítási folyamat ugyanaz, mint az atomokban (nem izotópokban) lévő neutronok számának meghatározásakor.
3 Keresse meg az atomtömeget. Izotópok esetében ezt nagyon könnyű megtenni, mivel az atomtömegük szerint nevezik őket. Esetünkben a 14C szén atomtömege 14. Most már tudjuk az izotóp atomtömegét; a későbbi számítási folyamat ugyanaz, mint az atomokban (nem izotópokban) lévő neutronok számának meghatározásakor.  4 Vonjuk le az atomszámot az atomtömegből. Mivel a protonok és a neutronok az atomtömeg abszolút részét teszik ki, az atomtömegből kivonva a protonok számát (vagyis az atomszámot, amely megegyezik a protonok számával), megadjuk az atomban lévő neutronok számát. Példánkban: 14 (atomtömeg) - 6 (protonok száma) = 8 (neutronok száma).
4 Vonjuk le az atomszámot az atomtömegből. Mivel a protonok és a neutronok az atomtömeg abszolút részét teszik ki, az atomtömegből kivonva a protonok számát (vagyis az atomszámot, amely megegyezik a protonok számával), megadjuk az atomban lévő neutronok számát. Példánkban: 14 (atomtömeg) - 6 (protonok száma) = 8 (neutronok száma). 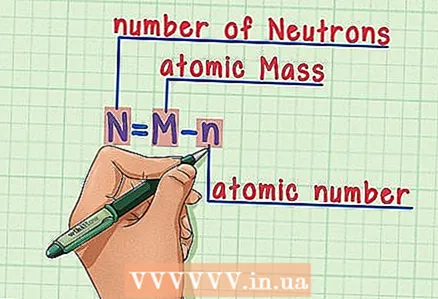 5 Ne feledje a képletet. A neutronok számának meghatározásához használja ezt a képletet:
5 Ne feledje a képletet. A neutronok számának meghatározásához használja ezt a képletet: - N = M - n
- N = neutronok száma
- M = atomtömeg
- n = atomszám
- N = M - n
Tippek
- A protonok és a neutronok alkotják az elemek szinte abszolút tömegét, míg az elektronok és más részecskék rendkívül jelentéktelen tömeget (ez a tömeg nullára hajlik).Mivel egy proton tömege körülbelül egy neutroné, és az atomszám a protonok száma, egyszerűen levonhatja a protonok számát a teljes tömegből.
- Az ozmium - szobahőmérsékleten szilárd állapotban lévő fém, nevét a görög "osme" szóból kapta - szag.
- Ha nem biztos abban, hogy mit jelent a periódusos rendszerben lévő szám, ne feledje: a táblázat általában egy atomszám (azaz a protonok száma) köré épül, amely 1 -nél kezdődik (hidrogén), és egy egységgel növekszik balról jobbra , 118 -al végződik (Oganesson). Ennek az az oka, hogy az atomban lévő protonok száma meghatározza magát az elemet, és ez a szám a legegyszerűbb módja az elemek rendszerezésének (például egy 2 protonnal rendelkező atom mindig hélium, akárcsak a 79 protont tartalmazó atom mindig arany ).