Szerző:
Judy Howell
A Teremtés Dátuma:
27 Július 2021
Frissítés Dátuma:
23 Június 2024

Tartalom
- Lépni
- 1. rész a 4-ből: A szerkezet megértése
- 2. rész a 4-ből: A szimbólum és a névadás megértése
- 3. rész a 4-ből: Az atomszám olvasása
- 4/4-es rész: Az atomtömeg leolvasása
Az elemek periódusos táblázata az eddig felfedezett 118 elem felsorolása. Számos szimbólum és szám jelzi az elemek különbségeit, míg a táblázat felépítése hasonlóságok szerint rendezi az elemeket. A periódusos táblázatot az alábbi útmutatások alapján olvashatja el.
Lépni
1. rész a 4-ből: A szerkezet megértése
 Gondoljon a periódusos rendszerre, mintha az bal felső sarokban kezdődne, és az utolsó sor végén, alul és jobbal végződne. A táblázat balról jobbra van felépítve növekvő atomszámok sorrendjében. Az atomszám az egyetlen atomban lévő protonok száma.
Gondoljon a periódusos rendszerre, mintha az bal felső sarokban kezdődne, és az utolsó sor végén, alul és jobbal végződne. A táblázat balról jobbra van felépítve növekvő atomszámok sorrendjében. Az atomszám az egyetlen atomban lévő protonok száma. - Nem minden sor vagy oszlop teljes. Bár lehet, hogy a központban hiányosságok vannak, olvassa tovább a táblázatot balról jobbra. Például a hidrogén 1. atomszámú, és a bal felső sarokban található. A hélium atomszáma 2, és a jobb felső sarokban található.
- Az 57–71 elemeket általában részhalmazként ábrázolják a táblázat jobb alsó sarkában. Ezek a "ritkaföldfém elemek".
 A táblázat minden oszlopában talál egy "elemcsoportot". 18 oszlop van.
A táblázat minden oszlopában talál egy "elemcsoportot". 18 oszlop van. - Használja a "csoport leolvasása" kifejezést, hogy felülről lefelé olvashasson.
- A számozást általában az oszlopok felett jelölik; azonban más csoportokba is sorolható, például a fémek.
- A periódusos rendszerben használt számozás nagyban különbözik. Ezek lehetnek római (IA), arab (1A) vagy az 1-18 számok.
- A hidrogén lehet a halogén családban és az alkálifémek, vagy mindkettő.
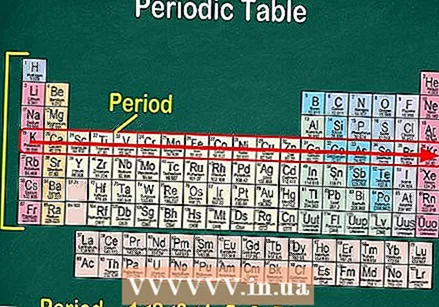 A táblázat minden sorában megtalálja az elemek "periódusait". 7 periódus van. Használja az "olvasás egy ponton" kifejezést balról jobbra olvasáshoz.
A táblázat minden sorában megtalálja az elemek "periódusait". 7 periódus van. Használja az "olvasás egy ponton" kifejezést balról jobbra olvasáshoz. - A periódusokat általában 1-től 7-ig számozzuk a táblázat bal oldalán.
- Minden periódus nagyobb, mint az utolsó. Ez összefügg a periódusos rendszerben szereplő atomok energiaszintjének növelésével.
 Ismerje meg a további csoportokat: fém, félfém és nem fém. A színek nagyban különböznek.
Ismerje meg a további csoportokat: fém, félfém és nem fém. A színek nagyban különböznek. - A Fémek csoportnak egy színe van. A hidrogénnek azonban gyakran ugyanaz a színe és csoportja, mint a nemfémeknek. A fémek fényesek, szobahőmérsékleten általában szilárdak, hőt és villamos energiát vezetnek, és képlékenyek és alakíthatók.
- A nemfémek színe azonos. Ezek a C-6-Rn-86 elemek, beleértve a H-1-et (hidrogén). Nincs fényük, vezetik a hőt és az áramot, és nem alakíthatók. Szobahőmérsékleten általában gázt képeznek, és lehetnek szilárd anyagok, gázok vagy folyadékok.
- A félfémek / metalloidok általában lila vagy zöld színűek, a másik két szín kombinációjaként. A vonal átlós, a B-5 elemektől az At-85-ig terjed. Bizonyos tulajdonságokkal rendelkeznek a fémek, más részük pedig a nem fémek.
 Ne feledje, hogy az elemeket néha a családok is felsorolják. Ezek az alkálifémek (1A), alkáliföldfémek (2A), halogének (7A), nemesgázok (8A) és szénatomok (4A).
Ne feledje, hogy az elemeket néha a családok is felsorolják. Ezek az alkálifémek (1A), alkáliföldfémek (2A), halogének (7A), nemesgázok (8A) és szénatomok (4A). - A számozás lehet római, arab vagy szabványos szám.
2. rész a 4-ből: A szimbólum és a névadás megértése
 Először olvassa el a szimbólumot. Ez egy vagy két betűből áll, és több nyelven szabványos.
Először olvassa el a szimbólumot. Ez egy vagy két betűből áll, és több nyelven szabványos. - A szimbólum származhat az elem latin nevéből vagy közös közös megnevezéséből.
- Sok esetben a szimbólum követi az angol elnevezési szokásokat, mint például a Hélium vagy a "He". Ez azonban nem szabály, amelyet feltételezhet. A vas például "Fe". Ezért a szimbólum / név kombinációra általában gyors emlékezetként emlékeznek.
 Nézd meg a közönséges nevet. Ez közvetlenül a szimbólum alatt van. Ez attól függ, hogy milyen nyelven íródott a periódusos rendszer.
Nézd meg a közönséges nevet. Ez közvetlenül a szimbólum alatt van. Ez attól függ, hogy milyen nyelven íródott a periódusos rendszer.
3. rész a 4-ből: Az atomszám olvasása
 Olvassa el a periódusos táblázatot az egyes elemek mezőjének középső részén található atomszám szerint. Mint korábban említettük, a rendszert balról fentről jobbra lent rendezik. Az atomszám ismerete a leggyorsabb módja annak, hogy több információt keressen az elemről.
Olvassa el a periódusos táblázatot az egyes elemek mezőjének középső részén található atomszám szerint. Mint korábban említettük, a rendszert balról fentről jobbra lent rendezik. Az atomszám ismerete a leggyorsabb módja annak, hogy több információt keressen az elemről. 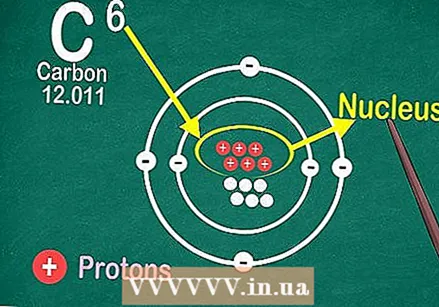 Az atomszám az elem egyetlen atomjának magjában lévő protonok száma.
Az atomszám az elem egyetlen atomjának magjában lévő protonok száma. Protonok hozzáadása vagy eltávolítása más elemet hoz létre.
Protonok hozzáadása vagy eltávolítása más elemet hoz létre. Az atomokban lévő protonok számának megismerése szintén meghatározza az elektronok számát. Az atomoknak annyi elektronja van, mint a protonoknak.
Az atomokban lévő protonok számának megismerése szintén meghatározza az elektronok számát. Az atomoknak annyi elektronja van, mint a protonoknak. - Ne feledje, hogy ez a szabály alól van kivétel. Amikor az atom elveszíti vagy megszerzi az elektronokat, elektromosan töltött ionokká válik.
- Ha van egy pluszjel az elem szimbóluma mellett, az azt jelzi, hogy pozitív töltésű. Mínusz szimbólummal negatívan töltődik fel.
- Ha nincs plusz vagy mínusz szimbólum, és a kémiai problémád nem az ionokkal kapcsolatos, akkor a protonok és az elektronok száma valószínűleg azonos.
4/4-es rész: Az atomtömeg leolvasása
 Határozza meg az atomtömeget. Ez az elem közös neve alatt található szám.
Határozza meg az atomtömeget. Ez az elem közös neve alatt található szám. - Bár úgy tűnhet, hogy az atomtömeg a rendszer bal felső sarkától a jobb alsóig növekszik, ez nem minden esetben igaz.
 Értse meg, hogy a legtöbb elemet tizedesjegyek jelölik. Az atomi tömeg a mag részecskéinek összessége; ez azonban a különböző izotópok súlyozott átlaga.
Értse meg, hogy a legtöbb elemet tizedesjegyek jelölik. Az atomi tömeg a mag részecskéinek összessége; ez azonban a különböző izotópok súlyozott átlaga.  Az atomtömeg segítségével megtalálja az egyes atomokban található neutronok számát. Az atomtömeg kerekítése a legközelebbi egész számra, a tömegszámra. Ezután kivonja a protonok számát a tömegszámból a neutronok számának meghatározásához.
Az atomtömeg segítségével megtalálja az egyes atomokban található neutronok számát. Az atomtömeg kerekítése a legközelebbi egész számra, a tömegszámra. Ezután kivonja a protonok számát a tömegszámból a neutronok számának meghatározásához. - Például: A vas atomtömege 55,847, tehát tömegszáma 56. Az elemnek 26 protonja van. Az 56 (tömegszám) mínusz 26 (proton) értéke 30. Egy vasatomban általában 30 neutron található.
- Az atomban lévő neutronok számának megváltoztatása izotópokat képez, amelyek az atom nehezebb vagy könnyebb változatai.



