Szerző:
Carl Weaver
A Teremtés Dátuma:
22 Február 2021
Frissítés Dátuma:
1 Július 2024
Tartalom
- Lépések
- 1. módszer a 2 -ből: Számítsa ki a moláris abszorpciós együtthatót a képlet segítségével
- 2. módszer 2 -ből: A moláris abszorpciós együttható grafikus megállapítása
- További cikkek
A moláris abszorpciós együttható, más néven moláris extinkciós együttható, azt méri, hogy az anyag kémiai részecskéi (molekulái) milyen erősen veszik el a fényt egy adott hullámhosszon. Minden anyagot saját moláris abszorpciós együttható jellemez, amely független a koncentrációtól és a térfogattól. Ezt a jellemzőt széles körben használják a kémiában, és nem szabad összetéveszteni az extinkciós együtthatóval, amelyet a fizikában gyakrabban használnak. A moláris abszorbancia standard mértékegysége liter, osztva mollal és centiméterenként (L mol cm).
Lépések
1. módszer a 2 -ből: Számítsa ki a moláris abszorpciós együtthatót a képlet segítségével
 1 Nézze meg a Bouguer-Lambert-Beer törvényt:A = ɛlc... A közegben a fény elnyelését az egyenlet írja le A = ɛlc, ahol A - egy bizonyos hullámhosszú fénymennyiség, amelyet a minta elnyelt, ɛ - moláris abszorpciós együttható, l a fény által megtett távolság az oldatban, és c - az oldat koncentrációja (a vizsgált molekulák száma térfogat egységben).
1 Nézze meg a Bouguer-Lambert-Beer törvényt:A = ɛlc... A közegben a fény elnyelését az egyenlet írja le A = ɛlc, ahol A - egy bizonyos hullámhosszú fénymennyiség, amelyet a minta elnyelt, ɛ - moláris abszorpciós együttható, l a fény által megtett távolság az oldatban, és c - az oldat koncentrációja (a vizsgált molekulák száma térfogat egységben). - Az abszorpciós együttható a standardon és a vizsgált mintán áthaladó fény intenzitásának arányából is megállapítható. Ebben az esetben az egyenlet a következő: A = napló10(ÉNo/ I).
- A fényerősséget spektrofotométerrel határozzák meg.
- Az oldat abszorpciós képessége a rajta áthaladó fény hullámhosszától függ. A hullámhossz bizonyos értékeinél a fény erősebben szívódik fel, mint másokon, és ezek az értékek az oldat összetételétől függenek. A számítás során ne felejtse el jelezni, hogy milyen hullámhosszra készülnek.
 2 A Bouguer-Lambert-Beer törvény átalakítása a moláris abszorpciós együttható kifejezésére. Ossza el az egyenlet mindkét oldalát hosszával és koncentrációjával, és az eredmény a moláris abszorpciós együttható kifejezése: ɛ = A / lc... Ennek a képletnek a segítségével kiszámíthatja a moláris abszorpciós együtthatót egy adott hullámhosszra.
2 A Bouguer-Lambert-Beer törvény átalakítása a moláris abszorpciós együttható kifejezésére. Ossza el az egyenlet mindkét oldalát hosszával és koncentrációjával, és az eredmény a moláris abszorpciós együttható kifejezése: ɛ = A / lc... Ennek a képletnek a segítségével kiszámíthatja a moláris abszorpciós együtthatót egy adott hullámhosszra. - Az elnyelő képesség rögzített távolságban az oldat koncentrációjától és a használt tartály alakjától függ. A moláris abszorpciós együttható kiküszöböli ezeket a tényezőket.
 3 Mérje meg a szükséges értékeket spektrofotometriával. Spektrofotométeren egy meghatározott hullámhosszú fényt vezetnek át egy anyagon, és a kibocsátott fény intenzitását mérik. A fény egy részét elnyeli az oldat, és a fényintenzitás csökken. A spektrofotométer méri az áteresztett fény intenzitását, amelyet a moláris abszorpciós együttható kiszámítására használnak.
3 Mérje meg a szükséges értékeket spektrofotometriával. Spektrofotométeren egy meghatározott hullámhosszú fényt vezetnek át egy anyagon, és a kibocsátott fény intenzitását mérik. A fény egy részét elnyeli az oldat, és a fényintenzitás csökken. A spektrofotométer méri az áteresztett fény intenzitását, amelyet a moláris abszorpciós együttható kiszámítására használnak. - Készítsen ismert koncentrációjú oldatot az elemzéshez c... Határozza meg a koncentrációt mol / gramm vagy mol / liter egységben.
- A meghatározáshoz l mérje meg a használt küvettát. Írd le a hosszát centiméterben.
- Mérje meg az abszorbanciát spektrofotométerrel A egy meghatározott hullámhosszra. A hullámhosszat méterben mérik, de a fény olyan rövid, hogy általában nanométerben (nm) fejezik ki. Az abszorpciós képesség dimenzió nélküli.
 4 Dugja be a számokat az egyenletbe, és keresse meg a moláris abszorpciós együtthatót. Vegyünk számszerű értékeket A, c és l és csatlakoztassa őket a képlethez ɛ = A / lc... Szorozz l a cmajd oszd meg A ennyivel meg kell találni a moláris abszorpciós együtthatót.
4 Dugja be a számokat az egyenletbe, és keresse meg a moláris abszorpciós együtthatót. Vegyünk számszerű értékeket A, c és l és csatlakoztassa őket a képlethez ɛ = A / lc... Szorozz l a cmajd oszd meg A ennyivel meg kell találni a moláris abszorpciós együtthatót. - Tegyük fel, hogy egy 0,05 mol / liter oldat abszorbanciáját mértük 1 cm -es küvettával. Ebben az esetben a 280 nm hullámhosszú fény fényelnyelése 1,5 volt. Hogyan lehet megtalálni a moláris abszorpciós együtthatót egy adott megoldáshoz?
- ɛ280 = A / lc = 1,5 / (1 x 0,05) = 30 L mol cm
- Tegyük fel, hogy egy 0,05 mol / liter oldat abszorbanciáját mértük 1 cm -es küvettával. Ebben az esetben a 280 nm hullámhosszú fény fényelnyelése 1,5 volt. Hogyan lehet megtalálni a moláris abszorpciós együtthatót egy adott megoldáshoz?
2. módszer 2 -ből: A moláris abszorpciós együttható grafikus megállapítása
 1 Mérje meg az áteresztett fény intenzitását az oldat különböző koncentrációihoz. Készítsen 3-4 különböző koncentrációjú oldatot.Spektrofotométerrel mérje meg a különböző koncentrációjú oldatok abszorbanciáját egy adott hullámhosszon. Kezdheti a legalacsonyabb koncentrációjú oldattal. A sorrend nem fontos, a legfontosabb, hogy ne keverjük össze és jegyezzük fel a mért abszorbanciaértékeket a koncentrációknak megfelelően.
1 Mérje meg az áteresztett fény intenzitását az oldat különböző koncentrációihoz. Készítsen 3-4 különböző koncentrációjú oldatot.Spektrofotométerrel mérje meg a különböző koncentrációjú oldatok abszorbanciáját egy adott hullámhosszon. Kezdheti a legalacsonyabb koncentrációjú oldattal. A sorrend nem fontos, a legfontosabb, hogy ne keverjük össze és jegyezzük fel a mért abszorbanciaértékeket a koncentrációknak megfelelően.  2 A kapott értékeket ábrázoljuk a grafikonon. Ábrázolja a koncentrációt a vízszintes X tengelyen és az abszorbanciát a függőleges Y tengelyen, és ábrázolja a méréseket pontokban.
2 A kapott értékeket ábrázoljuk a grafikonon. Ábrázolja a koncentrációt a vízszintes X tengelyen és az abszorbanciát a függőleges Y tengelyen, és ábrázolja a méréseket pontokban. - Rajzoljon egy vonalat a pontok közé. Ha a méréseket helyesen hajtották végre, a pontoknak egyenes vonalon kell feküdniük, mivel a Bouguer-Lambert-Beer törvény szerint az abszorpciós képesség közvetlenül arányos a koncentrációval.
 3 Definiálja egyenes lejtésáthaladva a kísérleti pontokon. Egy egyenes meredekségének megtalálásához ossza el az Y lépést az X abszcissza növekményével. Vegyen két pontot az egyenesen, vonja le az egyik pont megfelelő koordinátáit a másik koordinátáiból, és ossza el az Y különbséget az X különbséggel.
3 Definiálja egyenes lejtésáthaladva a kísérleti pontokon. Egy egyenes meredekségének megtalálásához ossza el az Y lépést az X abszcissza növekményével. Vegyen két pontot az egyenesen, vonja le az egyik pont megfelelő koordinátáit a másik koordinátáiból, és ossza el az Y különbséget az X különbséggel. - Az egyenes meredeksége (a meredekség vagy a lejtő érintője) a következőképpen található: (Y2 - Igen1) / (X2 - X1). Ebben az esetben az egyenes mentén magasabban elhelyezkedő ponthoz a 2 index, az alsó ponthoz pedig az 1 index tartozik.
- Tegyük fel, hogy 0,2 moláris koncentrációnál az abszorbancia 0,27, 0,3 koncentrációnál pedig 0,41 volt. Az abszorbanciát az Y tengelyen, a koncentrációt az X tengelyen ábrázoljuk. A fenti egyenlet segítségével keressük meg az egyenes meredekségét: (Y2 - Igen1) / (X2 - X1) = (0,41-0,27)/(0,3-0,2) = 0,14/0,1 = 1,4.
 4 A moláris abszorpciós együttható megtalálásához ossza el az egyenes meredekségét a fény által vezetett útvonallal (a küvettamélység). A fény által megtett út megegyezik a spektrofotométerben használt küvettamélységgel.
4 A moláris abszorpciós együttható megtalálásához ossza el az egyenes meredekségét a fény által vezetett útvonallal (a küvettamélység). A fény által megtett út megegyezik a spektrofotométerben használt küvettamélységgel. - Példánkban kapjuk: ha a meredekség 1,4, és a küvettamélység 0,5 centiméter, akkor a moláris abszorpciós együttható 1,4 / 0,5 = 2,8 L mol cm.
További cikkek
 Hogyan kell kiszámítani a négyzetmétert
Hogyan kell kiszámítani a négyzetmétert  Hogyan lehet megtalálni a protonok, neutronok és elektronok számát?
Hogyan lehet megtalálni a protonok, neutronok és elektronok számát?  Hogyan lehet meghatározni a vegyérték -elektronokat?
Hogyan lehet meghatározni a vegyérték -elektronokat?  Hogyan lehet kiegyensúlyozni a kémiai egyenleteket
Hogyan lehet kiegyensúlyozni a kémiai egyenleteket  Hogyan írhatjuk meg bármely elem atomjának elektronikus konfigurációját
Hogyan írhatjuk meg bármely elem atomjának elektronikus konfigurációját  Hogyan kell kiszámítani az oldat koncentrációját?
Hogyan kell kiszámítani az oldat koncentrációját?  Hogyan lehet kiszámítani a megoldás molaritását?
Hogyan lehet kiszámítani a megoldás molaritását?  Hogyan lehet megtalálni a neutronok számát egy atomban?
Hogyan lehet megtalálni a neutronok számát egy atomban?  Hogyan készítsünk ivóvizet sóból
Hogyan készítsünk ivóvizet sóból  A periódusos rendszer használata
A periódusos rendszer használata  Hogyan kell tárolni a száraz jeget
Hogyan kell tárolni a száraz jeget  Hogyan készítsünk száraz jeget
Hogyan készítsünk száraz jeget 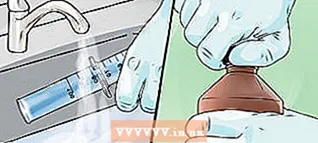 Hogyan készítsünk elefánt fogkrémet
Hogyan készítsünk elefánt fogkrémet  Hogyan kell hígítani az oldatot
Hogyan kell hígítani az oldatot