Szerző:
Clyde Lopez
A Teremtés Dátuma:
21 Július 2021
Frissítés Dátuma:
1 Július 2024

Tartalom
- Lépések
- 1. módszer a 2 -ből: A koncentrációk pontos kiszámítása
- 2. módszer 2 -ből: Egyszerű megoldások megszerzése gyakorlati célokra
- Figyelmeztetések
A hígítás következtében az oldat kevésbé koncentrálódik. Az oldatokat különböző okokból alacsonyabb koncentrációra hígítjuk (hígítjuk). A biokémikusok például koncentrált oldatokat hígítanak, hogy új oldatokat kapjanak, amelyeket aztán kísérleteik során felhasználnak. A csaposok viszont gyakran lágyabb vagy gyümölcslevekkel hígítják a szeszes italokat, hogy jó ízű koktélokat kapjanak. A hígítási arány kiszámításához használja a képletet C1V1 = C2V2ahol C.1 és C.2 az oldat kezdeti és végső koncentrációja, illetve V1 és V.2 - kezdeti és végső kötet.
Lépések
1. módszer a 2 -ből: A koncentrációk pontos kiszámítása
 1 Határozza meg, mit tud és mit nem. A kémiában a hígítás általában azt jelenti, hogy kis mennyiségű ismert koncentrációjú oldatot készítünk, majd semleges folyadékkal (például vízzel) hígítjuk, és így nagyobb térfogatú, kevésbé koncentrált oldatot kapunk. Ezt a műveletet nagyon gyakran használják kémiai laboratóriumokban, ezért a reagenseket a kényelem érdekében koncentrált formában tárolják, és szükség esetén hígítják. A gyakorlatban rendszerint ismert a kezdeti koncentráció, valamint a kapott oldat koncentrációja és térfogata; ahol ismeretlen térfogatú hígítandó koncentrált oldat.
1 Határozza meg, mit tud és mit nem. A kémiában a hígítás általában azt jelenti, hogy kis mennyiségű ismert koncentrációjú oldatot készítünk, majd semleges folyadékkal (például vízzel) hígítjuk, és így nagyobb térfogatú, kevésbé koncentrált oldatot kapunk. Ezt a műveletet nagyon gyakran használják kémiai laboratóriumokban, ezért a reagenseket a kényelem érdekében koncentrált formában tárolják, és szükség esetén hígítják. A gyakorlatban rendszerint ismert a kezdeti koncentráció, valamint a kapott oldat koncentrációja és térfogata; ahol ismeretlen térfogatú hígítandó koncentrált oldat. - Egy másik helyzetben, amikor például egy iskolai feladatot old meg a kémia területén, egy másik mennyiség ismeretlenként működhet: például a kezdeti térfogat és koncentráció megadásra kerül, és meg kell találni a végső oldat koncentrációját az ismert hangerő. Mindenesetre hasznos, ha a feladat megkezdése előtt leírjuk az ismert és ismeretlen mennyiségeket.
- Nézzünk egy példát. Tegyük fel, hogy 5 M koncentrációjú oldatot kell hígítani, hogy 1 -es koncentrációjú oldatot kapjunk mM... Ebben az esetben ismerjük a kiindulási oldat koncentrációját, valamint a kapott oldat térfogatát és koncentrációját; nem a kiindulási oldat térfogata, amelyet vízzel kell hígítani, ismert.
- Ne feledje: a kémiában M a koncentráció mértékegysége, más néven molaritás, ami megfelel az anyag mólszámának 1 liter oldatban.
 2 Csatlakoztassa az ismert értékeket a C képlethez1V1 = C2V2. Ebben a C képletben1 a kiindulási oldat koncentrációja, V1 - térfogata, C2 a végső oldat koncentrációja, és V2 - hangereje. A kapott egyenletből könnyen meghatározhatja a kívánt értéket.
2 Csatlakoztassa az ismert értékeket a C képlethez1V1 = C2V2. Ebben a C képletben1 a kiindulási oldat koncentrációja, V1 - térfogata, C2 a végső oldat koncentrációja, és V2 - hangereje. A kapott egyenletből könnyen meghatározhatja a kívánt értéket. - Néha hasznos, ha kérdőjelet tesz a keresett mennyiség elé.
- Térjünk vissza a példánkhoz. Az ismert értékeket helyettesítsük az egyenlőséggel:
- C1V1 = C2V2
- (5 M) V.1 = (1 mm) (1 l). A koncentrációknak különböző mértékegységei vannak. Maradjunk ennél kicsit részletesebben.
 3 Legyen tisztában a mértékegységek közötti eltérésekkel. Mivel a hígítás a koncentráció csökkenéséhez és gyakran jelentős csökkenéshez vezet, néha a koncentrációkat különböző egységekben mérik. Ha ezt elmulasztja, akkor több nagyságrenddel tévedhet az eredménnyel. Az egyenlet megoldása előtt konvertálja az összes koncentráció- és térfogatértéket ugyanarra a mértékegységre.
3 Legyen tisztában a mértékegységek közötti eltérésekkel. Mivel a hígítás a koncentráció csökkenéséhez és gyakran jelentős csökkenéshez vezet, néha a koncentrációkat különböző egységekben mérik. Ha ezt elmulasztja, akkor több nagyságrenddel tévedhet az eredménnyel. Az egyenlet megoldása előtt konvertálja az összes koncentráció- és térfogatértéket ugyanarra a mértékegységre. - Esetünkben két egységnyi koncentrációt használunk, M és mM. Fordítsunk le mindent M -re:
- 1 mM × 1 M / 1000 mM
- = 0,001 M.
- Esetünkben két egységnyi koncentrációt használunk, M és mM. Fordítsunk le mindent M -re:
 4 Oldjuk meg az egyenletet. Ha minden mennyiséget átváltott ugyanabba a mértékegységbe, megoldhatja az egyenletet. A megoldáshoz az egyszerű algebrai műveletek ismerete szinte mindig elegendő.
4 Oldjuk meg az egyenletet. Ha minden mennyiséget átváltott ugyanabba a mértékegységbe, megoldhatja az egyenletet. A megoldáshoz az egyszerű algebrai műveletek ismerete szinte mindig elegendő. - Példánkban: (5 M) V1 = (1 mm) (1 l). Mindent ugyanazokra az egységekre redukálva megoldjuk a V egyenletet1.
- (5 M) V.1 = (0,001 M) (1 L)
- V1 = (0,001 M) (1 L) / (5 M).
- V1 = 0,0002 l, vagy 0,2 ml.
- Példánkban: (5 M) V1 = (1 mm) (1 l). Mindent ugyanazokra az egységekre redukálva megoldjuk a V egyenletet1.
 5 Fontolja meg a megállapítások gyakorlatba való átültetését. Tegyük fel, hogy kiszámította a szükséges értéket, de még mindig nehéz a valódi megoldás elkészítése. Ez a helyzet teljesen érthető - a matematika és a tiszta tudomány nyelve néha távol áll a való világtól. Ha már ismeri mind a négy mennyiséget a C egyenletben1V1 = C2V2, a következőképpen járjon el:
5 Fontolja meg a megállapítások gyakorlatba való átültetését. Tegyük fel, hogy kiszámította a szükséges értéket, de még mindig nehéz a valódi megoldás elkészítése. Ez a helyzet teljesen érthető - a matematika és a tiszta tudomány nyelve néha távol áll a való világtól. Ha már ismeri mind a négy mennyiséget a C egyenletben1V1 = C2V2, a következőképpen járjon el: - Mérje meg a térfogatot V.1 oldatkoncentráció C1... Ezután adjuk hozzá a hígító folyadékot (vizet, stb.), Hogy az oldat térfogata V legyen2... Ennek az új megoldásnak a kívánt koncentrációja lesz (C2).
- Példánkban először 0,2 ml 5 M koncentrációjú törzsoldatot mérünk, majd vízzel 1 l térfogatra hígítjuk: 1 l - 0,0002 l = 0,9998 l, azaz 999,8 ml vizet hozzá. A kapott oldat szükséges koncentrációja 1 mM lesz.
2. módszer 2 -ből: Egyszerű megoldások megszerzése gyakorlati célokra
 1 Ellenőrizze a csomagoláson található információkat. Gyakran szükséges valamit hígítani a konyhában vagy más háztartási célokra. Például készítsen narancslevet koncentrátumból.A legtöbb esetben az elkészített termék csomagolása információkat tartalmaz ennek módjáról, gyakran részletes utasításokkal. Az utasítások olvasásakor ügyeljen a következőkre:
1 Ellenőrizze a csomagoláson található információkat. Gyakran szükséges valamit hígítani a konyhában vagy más háztartási célokra. Például készítsen narancslevet koncentrátumból.A legtöbb esetben az elkészített termék csomagolása információkat tartalmaz ennek módjáról, gyakran részletes utasításokkal. Az utasítások olvasásakor ügyeljen a következőkre: - a felhasznált termék térfogata;
- a folyadék térfogata, amelyben a terméket fel kell hígítani;
- folyadék típusa (általában víz);
- speciális tenyésztési utasításokat.
- Talán te nem információt talál a folyadék pontos mennyiségéről, mivel az ilyen információk feleslegesek a hétköznapi fogyasztók számára.
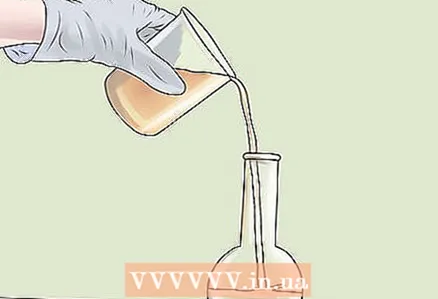 2 Adja hozzá a hígító folyadékot a tömény oldathoz. Otthon, például a konyhában csak a felhasznált koncentrátum térfogatát és a hozzávetőleges végtérfogatot kell tudnia. Hígítsa fel a koncentrátumot a szükséges mennyiségű folyadékkal, amelyet a hígítandó koncentrátum térfogata határoz meg. Ahol:
2 Adja hozzá a hígító folyadékot a tömény oldathoz. Otthon, például a konyhában csak a felhasznált koncentrátum térfogatát és a hozzávetőleges végtérfogatot kell tudnia. Hígítsa fel a koncentrátumot a szükséges mennyiségű folyadékkal, amelyet a hígítandó koncentrátum térfogata határoz meg. Ahol: - Ha például 1 csésze narancslé koncentrátumot az eredeti koncentráció 1/4 -ére kívánja hígítani, akkor hozzá kell adnia 3 csésze víz. Így a végső 4 csésze oldat egy csésze koncentrátumot vagy a teljes mennyiség 1/4-ét tartalmazza.
- Egy bonyolultabb példa: ha tenyészteni akar 2/3 csésze az eredeti koncentráció 1/4 -ére koncentráljon, adjon hozzá 2 csésze vizet, mivel a 2/3 csésze a 2 x 2/3 csésze teljes folyadékának 1/4 -e.
- Előzetesen győződjön meg arról, hogy az előkészített tartályok elegendőek -e a teljes végső folyadékmennyiség befogadására; használjon nagy csészét vagy tálat.
 3 Általában a koncentrátumpor térfogata figyelmen kívül hagyható. Általában kis mennyiségű por hozzáadása nem eredményez észrevehető változást a folyadék térfogatában. Más szóval, öntse a port a végső térfogatú folyadékba, és keverje össze.
3 Általában a koncentrátumpor térfogata figyelmen kívül hagyható. Általában kis mennyiségű por hozzáadása nem eredményez észrevehető változást a folyadék térfogatában. Más szóval, öntse a port a végső térfogatú folyadékba, és keverje össze.
Figyelmeztetések
- Tartsa be a gyártó által előírt biztonsági utasításokat vagy a vállalat előírásait. Ez különösen akkor fontos, ha savas oldatot hígít.
- Ha savas oldatokkal dolgozik, további hígítási és biztonsági utasításokra lesz szüksége.



