Szerző:
Louise Ward
A Teremtés Dátuma:
11 Február 2021
Frissítés Dátuma:
1 Július 2024

Tartalom
Az atom mérete olyan kicsi, hogy nehéz pontosan meghatározni egy kémiai vegyület atomszámát. Annak érdekében, hogy pontosan meg lehessen mérni egy anyagmennyiséget, a tudósok egy mólegységet használnak egy meghatározott számú atom képviseletére. Egy mól anyag meghatározása szerint egyenértékű a szénatomok számával 12 gramm szén-izotópban, ami körülbelül 6022x10 atom. Ezt az értéket Avogadro-számnak vagy Avogadro-állandónak hívják. Ezt nevezzük úgy is, hogy az atomok száma 1 mol bármely elemben található, és az anyag tömegének 1 molját az anyag moláris tömegének nevezzük.
Lépések
1/2 módszer: Számítsa ki az elem moláris tömegét
A moláris tömeg meghatározása. Az anyag moláris tömege az adott anyag egy móljának tömege (grammban). Egy elem moláris tömegének kiszámításához szorozzuk meg annak atomtömegét a gramm / mol konverziós faktorral (g / mol).
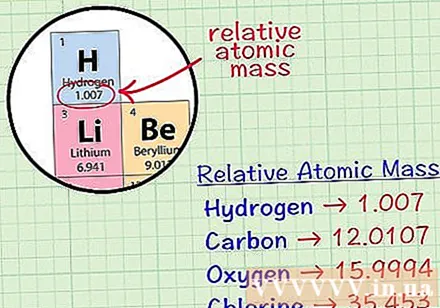
Keresse meg egy elem átlagos köbös atomját. Egy elem átlagos tömegatomja az átlagos tömeg, atomegységekben, egy mintában, amely az elem összes izotópját tartalmazza. Ezeket az információkat gyakran az elemek periódusos rendszerében adják meg. Egy elem megkeresésével megtalálja az átlagos kockaatomot, amely közvetlenül az elem kémiai szimbóluma alá van írva. Ez az érték nem egész szám, hanem tizedesjegyű szám.- Például hidrogénnel az átlagos tömegatom 1,007; Az átlagos köbméter szénatom 12,0107; Az oxigén átlagos tömegatomja 15,9994; a klór átlagos atomi tömege 35 453.

Szorozzuk meg az átlagos tömegatomot a moláris tömegállandóval. A moláris csúszás mértékegysége 0,001 kg / mol vagy 1 gramm / mol. Az átlagos tömegatom és a moláris tömegállandó szorzata az atomtömeg-egységet gramm / mol-ra konvertálja, így a hidrogén moláris tömege 1,007 gramm / mol, a szén esetében 12. Az oxigén értéke 0107 gramm / mol, az oxigén 15,9995 gramm / mol, a klóré pedig 35 453 gramm / mol.- Néhány elem a természetben molekulaként létezik, amelyek két vagy több azonos atomból állnak. Vagyis, ha meg akarja számolni az egynél több atomból álló vegyületek - például hidrogéngáz, oxigéngáz vagy klórgáz - moláris tömegét, meg kell határoznia a vegyület átlagos atomtömegét és meg kell szoroznia ezt az értéket. a moláris tömegállandóval, '' majd '' szorozza meg az imént talált terméket 2-vel.
- H-val2: 1,007 x 2 = 2,014 gramm / mol; mert O2: 15,9994 x 2 = 31,9988 gramm / mol; és Cl2: 35 453 x 2 = 70,096 gramm / mol.
2/2 módszer: Számítsa ki a vegyület moláris tömegét

Határozza meg a vegyület szerkezeti képletét! Az anyag szerkezeti képlete megadja az egyes vegyületek alkotóelemeinek atomszámát. (Ez az információ minden kézikönyvben elérhető). Például a sósav kémiai képlete HCl; a glükóz értéke C6H12O6. Ezzel a szerkezeti képlettel meghatározhatjuk a vizsgált vegyületet alkotó egyes atomtípusok számát.- Ahol a HCl-nek van egy hidrogénatomja és egy klóratomja.
- C glükózcukor molekula6H12O6 6 szénatom, 12 hidrogénatom és 6 oxigénatom van.
Határozza meg az egyes alkotóelemek átlagos tömegatomját. A periódusos táblázattal keresse meg a vegyületben található egyes elemek átlagos tömegatomját. Az átlagos tömegatomot általában a periódusos rendszer kémiai szimbóluma alá írják. Hasonlóan az elem moláris tömegének kiszámításához, az átlagos tömegatomot szorozzuk meg 1 gramm / mol értékkel.
- A sósavat képző elemek átlagos tömegatomja a következő: hidrogén 1007 g / mol és klór 35,453 g / mol.
- A glükózmolekulát alkotó elemek átlagos tömegatomja: szén: 12,017 g / mol; hidrogén, 1,007 g / mol; és oxigén 15,9995 g / mol.
Számítsa ki az egyes komponensek moláris tömegét. Ha egy elem tömegatomját megszorozzuk egy vegyületben részt vevő atomok számával, megkapjuk az elem átlagos tömegét a vegyületben.
- Sósav, HCl esetében a hidrogén elem moláris tömege 1,007 g / mol, a klóré pedig 35,453 g / mol.
- A glükóz esetében a C6H12O6az egyes elemek moláris tömege a következő: szén, 12,0107 x 6 = 72,0642 g / mol; hidrogén, 1007x12 = 12,084 g / mol; oxigén, 15,9995 x 6 = 95,9964 g / mol.
Az alkotó elemek összes moláris tömege. A komposztáló elemek teljes moláris tömege a vegyület moláris tömege.Az előző lépésben kiszámoltuk a vegyületben lévő egyes elemek moláris tömegét, ebben a lépésben csak ezeket az értékeket kell összeadnunk.
- A sósav moláris tömege 1007 + 35 453 = 36 460 g / mol. 36,46 gramm 1 mol sósav tömege.
- A glükóz moláris tömege 72,0642 + 12,084 + 95,9964 = 180,1446 g / mol. Tehát minden mol glükóz tömege 180,14 gramm.
Tanács
- Bár az esetek többségében az átlagos tömegatomot 1000 rész pontossággal (4 tizedesjegyig) rögzítik, a laboratóriumokban a moláris tömeget gyakran 2 tizedesjegyre csökkentik, néha még kevésbé, nagy molekulák esetén. Ezért laboratóriumi esetben a sósav moláris tömege 36,46 g / mol, a glükóz esetében 180,14 g / mol.
Amire szükséged van
- Kémiai referenciakönyv vagy periódusos rendszer
- Számítógép