Szerző:
Robert Simon
A Teremtés Dátuma:
24 Június 2021
Frissítés Dátuma:
1 Július 2024

Tartalom
Az elméleti hozam egy olyan kifejezés, amelyet a kémia használ az anyag maximális mennyiségére, amelyet elvár egy kémiai reakciótól. A reakcióegyenlet kiegyensúlyozásával és a korlátozó reagens meghatározásával kezdheti. Amikor megméri a használni kívánt reagens mennyiségét, kiszámíthatja a kapott anyag mennyiségét. Ez az egyenlet elméleti hozama. Egy tényleges kísérlet során valószínűleg veszít belőle, mert ez nem ideális kísérlet.
Lépni
1/2 rész: A korlátozó reagens meghatározása
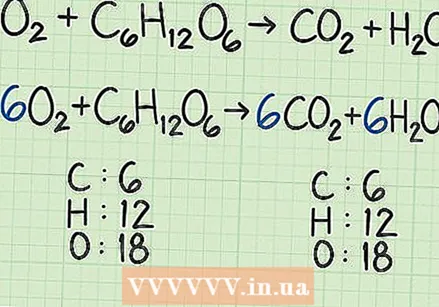 Kezdje egyensúlyi reakcióval. A reakcióegyenlet hasonló a recepthez. Megmutatja, hogy mely reagensek (bal oldalon) reagálnak egymással termékeket képezve (a jobb oldalon). Egy egyensúlyi reakciónak ugyanannyi atomja lesz az egyenlet bal oldalán (mint reagensek), mint a jobb oldalán (termékek formájában).
Kezdje egyensúlyi reakcióval. A reakcióegyenlet hasonló a recepthez. Megmutatja, hogy mely reagensek (bal oldalon) reagálnak egymással termékeket képezve (a jobb oldalon). Egy egyensúlyi reakciónak ugyanannyi atomja lesz az egyenlet bal oldalán (mint reagensek), mint a jobb oldalán (termékek formájában). - Tegyük fel például, hogy megvan az egyszerű egyenlet
 Számítsa ki az egyes reakciók moláris tömegét. A periódusos rendszer vagy más referenciakönyv segítségével keresse meg az egyes összetevők egyes atomjainak moláris tömegét. Adja össze őket, hogy megkapja a reagensek mindegyikének moláris tömegét. Tegye ezt a vegyület egyetlen molekulájára. Vizsgáljuk meg újra az oxigén és a glükóz szén-dioxiddá és vízzé történő átalakulásának egyenletét:
Számítsa ki az egyes reakciók moláris tömegét. A periódusos rendszer vagy más referenciakönyv segítségével keresse meg az egyes összetevők egyes atomjainak moláris tömegét. Adja össze őket, hogy megkapja a reagensek mindegyikének moláris tömegét. Tegye ezt a vegyület egyetlen molekulájára. Vizsgáljuk meg újra az oxigén és a glükóz szén-dioxiddá és vízzé történő átalakulásának egyenletét: 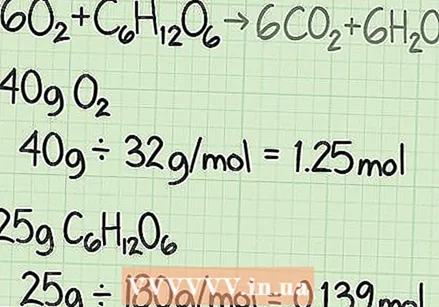 Konvertálja az egyes reagensek mennyiségét grammról molra. Egy valódi kísérlethez ismert lesz az összes alkalmazott reagens tömege grammban. Osszuk el ezt az értéket az anyag moláris tömegével, a molok számára átszámítva.
Konvertálja az egyes reagensek mennyiségét grammról molra. Egy valódi kísérlethez ismert lesz az összes alkalmazott reagens tömege grammban. Osszuk el ezt az értéket az anyag moláris tömegével, a molok számára átszámítva. - Tegyük fel például, hogy 40 gramm oxigénnel és 25 gramm glükózzal kezdi.
- 40 g
 Határozza meg a reagensek moláris arányát. Az anyajegy egy számítási eszköz, amelyet a kémiában használnak a molekulák tömegük alapján történő számlálására. Az oxigén és a glükóz molok számának meghatározásával tudja, hogy mindegyikből hány molekula indul ki. Mindkettő arányának megtalálásához ossza el az egyik reagens mólszámát a másikéval.
Határozza meg a reagensek moláris arányát. Az anyajegy egy számítási eszköz, amelyet a kémiában használnak a molekulák tömegük alapján történő számlálására. Az oxigén és a glükóz molok számának meghatározásával tudja, hogy mindegyikből hány molekula indul ki. Mindkettő arányának megtalálásához ossza el az egyik reagens mólszámát a másikéval. - A következő példában 1,25 mol oxigénnel és 0,139 mol glükózzal kezdi. Tehát az oxigén és a glükóz molekulák aránya 1,25 / 0,139 = 9,0. Ez az arány azt jelenti, hogy kilencszer annyi oxigénmolekula van, mint a glükózban.
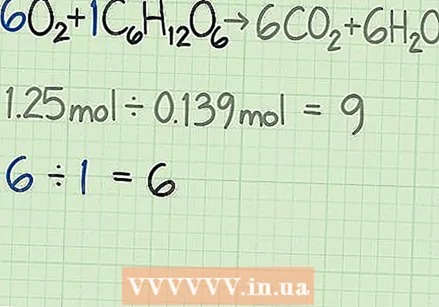 Határozza meg a reakció ideális arányát. Nézze meg az egyensúlyi választ. Az egyes molekulák együtthatói megmondják, hogy mekkora arányban szükségesek a reakciók. Ha pontosan a képlet által megadott arányt használja, akkor mindkét reagenst egyformán kell használni.
Határozza meg a reakció ideális arányát. Nézze meg az egyensúlyi választ. Az egyes molekulák együtthatói megmondják, hogy mekkora arányban szükségesek a reakciók. Ha pontosan a képlet által megadott arányt használja, akkor mindkét reagenst egyformán kell használni. - Ehhez a reakcióhoz a reagenseket mint
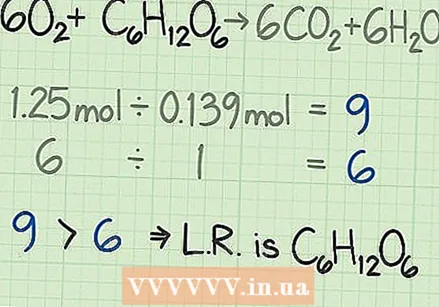 Hasonlítsa össze az arányokat a korlátozó reagens megtalálásához. A legtöbb kémiai reakcióban az egyik reagens hamarabb elhasználódik, mint a másik. Az elsőként felhasznált reagenst korlátozó reagensnek nevezzük. Ez a korlátozó reagens meghatározza, hogy a kémiai reakció meddig folytatódhat, és az elméleti hozamra számíthat. Hasonlítsa össze a határérték-reagens meghatározásához kiszámított két arányt:
Hasonlítsa össze az arányokat a korlátozó reagens megtalálásához. A legtöbb kémiai reakcióban az egyik reagens hamarabb elhasználódik, mint a másik. Az elsőként felhasznált reagenst korlátozó reagensnek nevezzük. Ez a korlátozó reagens meghatározza, hogy a kémiai reakció meddig folytatódhat, és az elméleti hozamra számíthat. Hasonlítsa össze a határérték-reagens meghatározásához kiszámított két arányt: - A következő példában kilencszer annyi oxigénnel indul, mint a glükóz, molban mérve. A képlet azt mondja neked, hogy az ideális arányod hatszor több oxigént és glükózt tartalmaz. Tehát több oxigénre van szüksége, mint glükózra. Tehát a másik reagens, ebben az esetben a glükóz, a korlátozó reagens.
- Ehhez a reakcióhoz a reagenseket mint
- Tegyük fel például, hogy megvan az egyszerű egyenlet
2. rész: Az elméleti hozam meghatározása
 Tekintse meg a választ, hogy megtalálja a kívánt terméket. A kémiai egyenlet jobb oldala a reakciótermékeket mutatja. Ha a reakció kiegyensúlyozott, az egyes termékek együtthatói jelzik, hogy az egyes molekuláris arányok közül hányra számíthat. Minden terméknek van elméleti hozama, vagy az a termékmennyiség, amelyre a reakció teljes befejezése után számíthat.
Tekintse meg a választ, hogy megtalálja a kívánt terméket. A kémiai egyenlet jobb oldala a reakciótermékeket mutatja. Ha a reakció kiegyensúlyozott, az egyes termékek együtthatói jelzik, hogy az egyes molekuláris arányok közül hányra számíthat. Minden terméknek van elméleti hozama, vagy az a termékmennyiség, amelyre a reakció teljes befejezése után számíthat. - A fenti példával folytatva elemzi a választ
 Jegyezze fel a korlátozó reagens mólszámát. Mindig össze kell hasonlítania a korlátozó reagens móljainak számát a termék móljainak számával. Ha megpróbálja összehasonlítani mindegyik tömegét, nem kapja meg a helyes eredményt.
Jegyezze fel a korlátozó reagens mólszámát. Mindig össze kell hasonlítania a korlátozó reagens móljainak számát a termék móljainak számával. Ha megpróbálja összehasonlítani mindegyik tömegét, nem kapja meg a helyes eredményt. - A fenti példában a glükóz a korlátozó reagens. Móltömeg-számítások szerint az első 25 g glükóz 0,139 mol glükóznak felel meg.
 Hasonlítsa össze a termékben lévő molekulák és a reagens arányát. Térjünk vissza az egyensúlyi reakcióhoz. Ossza el a kívánt termék molekuláinak számát a korlátozó reagens molekuláinak számával.
Hasonlítsa össze a termékben lévő molekulák és a reagens arányát. Térjünk vissza az egyensúlyi reakcióhoz. Ossza el a kívánt termék molekuláinak számát a korlátozó reagens molekuláinak számával. - Az egyensúlyi reakció ebben a példában az
 Szorozzuk meg ezt az arányt a korlátozó reagens mólszámával. A válasz a kívánt termék elméleti hozama molban.
Szorozzuk meg ezt az arányt a korlátozó reagens mólszámával. A válasz a kívánt termék elméleti hozama molban. - Ebben a példában a 25 g glükóz 0,139 mol glükóznak felel meg. A szén-dioxid és a glükóz aránya 6: 1. Arra számít, hogy képes lesz hatszor annyi mol széndioxidot előállítani, mint ahány mól glükózzal kezdte.
- A szén-dioxid elméleti hozama (0,139 mol glükóz) x (6 mol szén-dioxid / mol glükóz) = 0,834 mol szén-dioxid.
 Konvertálja az eredményt grammra. Ez az előző lépés fordítottja a molok számának vagy a reagens mennyiségének kiszámításához. Ha ismeri a várható mólok számát, szorozza meg ezt a termék moláris tömegével, hogy megtalálja az elméleti hozamot grammban.
Konvertálja az eredményt grammra. Ez az előző lépés fordítottja a molok számának vagy a reagens mennyiségének kiszámításához. Ha ismeri a várható mólok számát, szorozza meg ezt a termék moláris tömegével, hogy megtalálja az elméleti hozamot grammban. - A következő példában a CO moláris tömege látható2 körülbelül 44 g / mol. (A szén moláris tömege ~ 12 g / mol, az oxigén pedig ~ 16 g / mol, tehát az összes 12 + 16 + 16 = 44).
- Szorozzon 0,834 mol CO-t2 x 44 g / mol CO2 = ~ 36,7 gramm. A kísérlet elméleti hozama 36,7 gramm CO2.
 Ha szükséges, ismételje meg a számítást a másik termékkel. Számos kísérletben csak egy adott termék hozama érdekelhet. Ha meg akarja ismerni mindkét termék elméleti hozamát, akkor csak annyit kell tennie, hogy megismétli a folyamatot.
Ha szükséges, ismételje meg a számítást a másik termékkel. Számos kísérletben csak egy adott termék hozama érdekelhet. Ha meg akarja ismerni mindkét termék elméleti hozamát, akkor csak annyit kell tennie, hogy megismétli a folyamatot. - Ebben a példában a víz a második termék
. Az egyensúlyi reakció szerint hat molekula vízre számíthat egy glükózmolekulától. Ez 6: 1 arányú. Tehát 0,139 mol glükóznak 0,834 mol vizet kell eredményeznie.
- Szorozzuk meg a vízmólok számát a víz moláris tömegével. A moláris tömeg 2 + 16 = 18 g / mol. A szorzattal szorozva 0,139 mol H-t kapunk2O x 18 g / mol H2O = ~ 2,50 gramm. A kísérlet elméleti vízhozama 2,50 gramm.
- Ebben a példában a víz a második termék
- Az egyensúlyi reakció ebben a példában az
- A fenti példával folytatva elemzi a választ